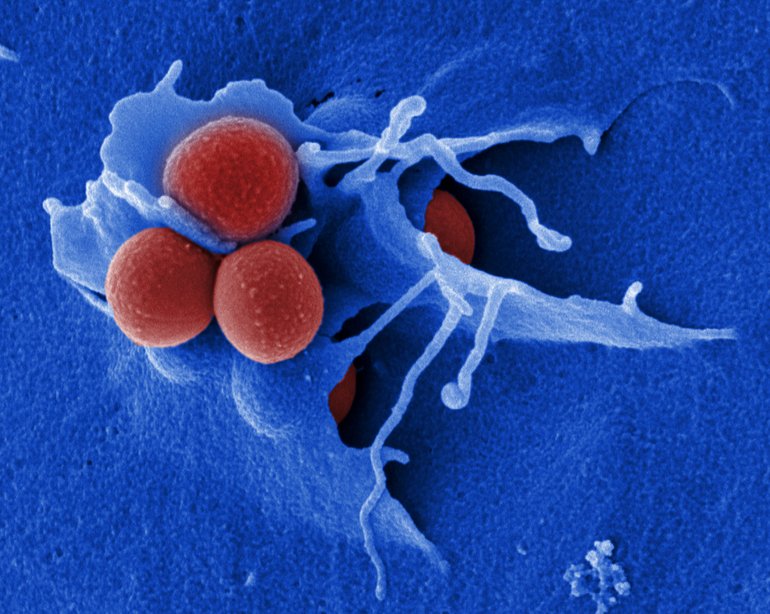
Forscher analysieren, unter welchen Voraussetzungen sich Antivirulenz-Strategien auf multiresistente Keime anwenden lassen. Ein erfolgreicher Einsatz scheint vor allem im Rahmen einer personalisierten Infektionsmedizin möglich sein.
Infektionen mit multiresistenten Keimen nehmen weltweit zu, was zu schweren Komplikationen etwa bei Gelenkoperationen, in der Chemotherapie oder bei der Versorgung von Frühchen führen kann. Bereits jetzt sterben weltweit mehr als 700 000 Menschen pro Jahr an Infektionen mit resistenten Erregern. Viele Forscher arbeiten deshalb an neuen Antibiotika und alternativen antimikrobiellen Medikamenten. Eine besonders attraktive Option ist die Antivirulenz-Therapie. Sie zielt darauf ab, die Eigenschaften eines Erregers, die eine erfolgreiche Besiedlung des Wirtes ermöglichen – so genannte Virulenzfaktoren – durch spezifische Arzneistoffe direkt im Körper abzuschwächen. Der Erreger selbst bleibt dabei am Leben.
Konkret werden zum Beispiel Haftmoleküle oder die Kommunikationsschnittstellen der Bakterien – so genannte Quorum-Sensing-Signale – blockiert. Wissenschaftler arbeiten daran, mithilfe dieser Strategie bakterielle Krankheitserreger während der Infektion so zu stören, dass sie nicht in der Lage sind, den Wirtsorganismus effektiv zu besiedeln und Infektionen auszulösen.
Fehlender Selektionsdruck
„Durch die Antivirulenz-Therapie wird das Immunsystem des Wirtes in die Lage versetzt, die Infektion mit dem abgeschwächten Erreger selbst oder mit Unterstützung eines Antibiotikums zu besiegen“, sagt Prof. Eva Medina, Leiterin der Abteilung Infektionsimmunologie am Helmholtz-Zentrum für Infektionsforschung (HZI) in Braunschweig. „Da die Keime am Leben und vermehrungsfähig bleiben, entsteht kein Selektionsdruck, wodurch wiederum eine Resistenzbildung verhindert werden soll.“
Das Konzept der Antivirulenz-Therapie stecke allerdings noch in den Kinderschuhen und es seien weitere umfangreiche Forschungsarbeiten notwendig, um es in die Praxis zu überführen. „Ein sehr wichtiger Aspekt, der bei der Entwicklung neuer Antivirulenz-Konzepte berücksichtigt werden muss, ist die Tatsache, dass sich die krankmachenden Eigenschaften eines Erregers nicht immer gleich ausbilden“, sagt Medina. „Die spezifische Ausprägung dieser Eigenschaften wird stark durch die direkte Umgebung während der Infektion beeinflusst.“ Es sei daher wichtig zu verstehen, welchen Einfluss die spezifische Immunantwort des einzelnen Individuums auf die Genaktivität eines Krankheitserregers hat. Dies haben die Wissenschaftler am HZI jetzt am Beispiel des bedeutenden Krankenhauskeims Staphylococcus aureus und an Mäusen untersucht.
Virulenz hängt vom Individuum ab
Sie konnten nachweisen, dass sich Unterschiede in der Immunantwort von Mäusen und die daraus resultierenden unterschiedlichen Krankheitsverläufe stark auf die Ausprägung der spezifischen Virulenz eines Erregers auswirkten. Eva Medina erklärt: „Die bei Mäusen bestehende Variabilität gegenüber Staphylococcus-Bakterien wird auch bei Menschen beobachtet und resultiert unter anderem aus Unterschieden des Alters oder der spezifischen genetischen Ausstattung.“ Dass es vom Wirt abhängt, wie stark die Virulenzfaktoren von Krankheitserregern ausgeprägt werden, könnte eine effektive Anwendung von Antivirulenz-Therapien jedoch auch limitieren. „Dies ist eine sehr wichtige Information aus der Studie, um funktionierende Antivirulenz-Konzepte zu entwickeln“, sagt Eva Medina. „Im besten Fall sind die krankmachenden Faktoren der Bakterien, auf die künftige Therapien abzielen sollen, nicht wirtsabhängig.“ Anderenfalls müsse die Antivirulenz-Strategie für verschiedene Patienten individuell angepasst werden.
Unsere Whitepaper-Empfehlung
Lesen Sie, warum Medizintechnikunternehmen ihre Testprozesse für die Validierung von Software optimieren müssen und wie sie dabei die Erfahrung der Automobilbranche für sich nutzen können.
Teilen: