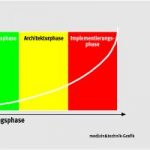
Auch wenn der Zertifizierer nicht beraten darf, kann er schon im Entwicklungsprozess bei einer Preliminary Investigation auf drohende Probleme hinweisen. Das vermeidet unangenehme Überraschungen bei der Zulassung.
Wenn im Laufe eines Entwicklungsprojektes Redesigns erforderlich werden, weil rechtliche Vorgaben nicht ausreichend berücksichtigt wurden, fallen nicht nur die tatsächlichen Kosten für das Überarbeiten eines fertig entwickelten Röntgen-C-Bogens, eines HF-Chirurgie- oder Ultraschallgerätes an: Eine verzögerte Markteinführung wirkt sich bis zu Beträgen in Milionenhöhe negativ auf den Umsatz aus.
Eine Möglichkeit, sich vor solchen Überraschungen zu schützen, ist die so genannte entwicklungsbegleitende Prüfung, die auch unter dem Begriff Preliminary Investigation bekannt ist: Hierfür sucht das entwickelnde Unternehmen schon in einer sehr frühen Phase der Produktentwicklung den Kontakt zu einem Prüfingenieur. Ihm werden die bis dahin vorhandenen Unterlagen vorgelegt, die er auf Konflikte mit den rechtlichen Vorgaben der Zielmärkte hin überprüft.
Damit ist keine Beratung im engeren Sinne gemeint – eine solche Beratung durch eine Zulassungsstelle ist gesetzlich verboten, da sie zu Interessenskonflikten führen kann. Möglich und erlaubt ist es aber, beispielsweise die Zulassungsdokumentation daraufhin zu prüfen, ob sie formal und inhaltlich richtig ist. Dann zeigt sich schon, ob eventuell ein Bauteil eingeplant ist, das einer Norm widerspricht. Darauf darf der Prüfingenieur aufmerksam machen, und der Hersteller kann Alternativen vorschlagen.
Ein typisches Beispiel dafür, was bei einer entwicklungsbegleitenden Prüfung zu berücksichtigen wäre, ist der Brandschutzaspekt bei Produkten, die – wie für Medizinprodukte häufig – in den USA oder Kanada eingesetzt werden sollen. Auf Grund der dort üblichen Gebäudebauweise gehört er zu den wichtigsten Anforderungen des nordamerikanischen Marktes. Dennoch bleiben die relevanten Bestimmungen des National Electrical Code, NFPA 70 (NEC) und der Standard for Health Care Facilities NFPA 99 in den frühen Phasen der Entwicklung oft unberücksichtigt. Ein weiteres Beispiel für entwicklungsbegleitende Prüfung ist die Softwaredokumentation: Eine Betrachtung zeigt, ob diese den Normen IEC 60601-1-4 oder ISO62304 entspricht.
Diese Themen betreffen aber nicht nur die Hersteller von Medizingeräten, sondern zunehmend auch ihre mittelständischen Zulieferer. Je komplexer die Lieferketten sind, desto wichtiger ist es, für den internationalen Markt gerüstet zu sein. Jede mechanische und elektrotechnische Komponente muss schließlich den Sicherheitsanforderungen des Zielmarktes entsprechen.
Wie so eine entwicklungsbegleitende Prüfung organisatorisch aussieht, kann der Hersteller eines Medizinproduktes beeinflussen: So entscheidet er, welche Bereiche des Unternehmens involviert sein sollen und ob Teile der Preliminary Investigation, die an einem Produkt durchgeführt wurde, auch für die Schulung seiner Mitarbeiter verwandt werden sollen. Auch Zulieferbetriebe, die am Projekt mitarbeiten, können einbezogen werden. Die Dauer der Prüfung hängt natürlich davon ab, wie komplex das Produkt ist und ob die Dokumentation noch lückenhaft oder weitgehend vollständig ist. Das lässt sich aber in der Regel im Vorfeld von Hersteller und Zertifizierer gemeinsam abschätzen.
Der optimale Zeitpunkt für die Kontaktaufnahme zum Zertifizierungsunternehmen ist sicher schwer zu definieren. Grundsätzlich kann er in jeder Phase der Entwicklung aufgebaut werden. Dabei kann, je nach Bedarf, eine generelle Schulung der Entwickler sinnvoll sein oder eine frühzeitige Entwicklungsbegleitung. Um aber den Anteil der Nichtkonformitäten so gering wie möglich zu halten, ist es sicher empfehlenswert, den Kontakt schon in der Anforderungsphase herzustellen und die bis dahin vorhandenen Entwicklungsunterlagen analysieren zu lassen.
Sinnvoll wäre es, solche Überlegungen sogar als Baustein in ein nach ISO13485 entwickeltes Qualitätsmanagementsystem aufzunehmen. Doch weisen die meisten dieser QM-Systeme bislang nicht auf die Notwendigkeit hin, im Designprozess die Meinung von Zertifizierungsspezialisten einzuholen, Vorabprüfungen der Nullserie einzuplanen oder, besser noch, schon die ersten Konzepte und Pläne einer entwicklungsbegleitenden Prüfung zu unterziehen.
Bislang sind sich vor allem die Großunternehmen dieser Zusammenhänge bewusst und binden mitunter bereits den Zertifizierungsdienstleister im Vorfeld ein. Aber auch für mittelständische Unternehmen oder gar eine Fünf-Mann-Firma kann eine entwicklungsbegleitende Prüfung eine sinnvolle Hilfestellung sein. Denn bisher zeigt der Alltag bei der Zertifizierung, dass ein erheblicher Anteil der zur Zulassung vorgestellten Geräte geringe bis gravierende Abweichungen gegenüber der anzuwendenden Produktnorm aufweist.
Neben dem Vermeiden der Kosten für ein Redesign kann die entwicklungsbegleitende Prüfung den Herstellern also auch schon frühzeitig den Schrecken vor dem Zulassungsprozess nehmen: Sie fördert das Verständnis und das Wissen um die Auslegung der Normen im Einklang mit den Anforderungen des Marktes.
Joachim M. Hochhaus Medical Technical Manager EULA bei Underwriters Laboratories (UL) in Neu-Isenburg
Ihr Stichwort
• Produktentwicklung
• Rechtliche Vorgaben
• Verschiedene Zielmärkte • Nutzen von Expertise
Unsere Whitepaper-Empfehlung
Gewährleisten Sie Sterilität bei Medizinprodukten, wie Implantaten und OP-Material. Das Whitepaper von BGS Beta-Gamma-Service gibt Einblicke in den Ablauf, Vorteile, Validierungsschritte der Strahlensterilisation & wichtige Aspekte beim Wechsel des Sterilisationsverfahrens. Jetzt…
Teilen: