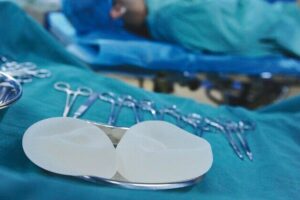
TÜV Süd hat noch Kapazitäten frei für Konformitätsbewertungsverfahren von Medizinprodukten mit der Medical Device Regulation (MDR) und der In Vitro Diagnostic Regulation (IVDR). Im Zuge der Engpässe hat die Benannte Stelle rechtzeitig Personal aufgebaut.
Recht
Mit dem AI Act schafft die EU regulatorische Klarheit über grundsätzliche Regeln für das Inverkehrbringen von Produkten mit Künstlicher Intelligenz (KI)...
Wie sich die neue EU-Verordnung zu Künstlicher Intelligenz, der AI Act, auf die Medizintechnik auswirkt, hängt von der konkreten Umsetzung in Deutschland ab...
Um langfristig auf internationalen Medtech-Märkten erfolgreich zu sein, müssen Unternehmen Synergien zwischen den regulatorischen Systemen nutzen. Einen Weg...
Ein ausgewogenes Verhältnis von Patientensicherheit zu umsetzbaren Vorgaben für Hersteller – das ist der Kern des Appells, den die German Health Alliance...
Grundsätzlich ist gemäß der Medical Device Regulation in der EU die Aufbereitung von Einmal-Medizinprodukten erlaubt. Es gibt dafür zwei Verfahren: nach...
Produkte ohne medizinische Zweckbestimmung waren von bisherigen EU-Regularien nicht erfasst. Mit dem Annex XVI in der EU-Medizinprodukteverordnung (MDR)...
Um Unternehmen bei Fragen der Marktzulassung medizintechnischer Produkte zu unterstützen, hat die Hochschule Pforzheim ein Kompetenzzentrum errichtet. Partner...
Das Hinweisgeber-Schutzgesetz (HinSchG) schützt Whistleblower. Es ist Anfang Juli 2023 in Kraft getreten. Auch für die Medizintechnik heißt das: In...
Das Lieferketten-Sorgfaltspflichten-Gesetz stellt die unternehmerische und soziale Verantwortung der Lieferanten in den Vordergrund. Auch...
Verpackungsgesetz | Auch Medizinprodukte unterliegen den rechtlichen Bestimmungen des Verpackungsgesetzes, dessen Regelungen 2022 noch einmal verschärft...
Ob maschinelles Lernen, künstliche Intelligenz oder Augmented Reality, allen gemeinsam ist ihr großes Potenzial, die Medizintechnik zu revolutionieren. Damit...
Die neue EU-MDR bildet die Entwicklung von immer stärker vernetzter Technologie und die daraus resultierenden Risiken ab: Die IT-Sicherheit in...
Am 6. Januar veröffentlichte die EU-Kommission einen Vorschlag zur Änderung der Medizinprodukteverordnung (MDR) und der Verordnung über In-vitro-Diagnostika...
Ab Januar gilt in Deutschland das Lieferkettensorgfaltspflichtengesetz, das indirekt auch kleinere Unternehmen zu Fragen von Menschenrechtsverletzungen in die...
Wie lässt sich ein Managementsystem für die Informationssicherheit – das für Diga vorgeschrieben ist – in ein Qualitätsmanagementsystem integrieren...
Welche Anforderungen muss das Qualitätsmanagement erfüllen, wenn Produkte additiv gefertigt werden? Bis Ende 2022 soll das in der Norm ISO/ASTM 52920...
Gesetze, Normen, Guidances, der Stand der Technik: Bevor ein Medizinprodukt auf den Markt kommen kann, müssen viele Details berücksichtigt werden. Für...
Eine Zusammenarbeit der ungewohnten Art will die Osypka AG in Rheinfelden in Zukunft – nicht nur – mit Start-ups aus der Medizintechnik erproben. Auch beim...
Bei der EU-Verordnung zum Health Technology Assessment (HTA) geht es darum, den medizinischen Nutzen eines Produktes mit anderen Produkten oder...
Eine umfassende Checkliste zu MDR-Anforderungen an eine KI hat die Interessengemeinschaft der Benannten Stellen für Medizinprodukte in Deutschland (IG-NB)...
Ein Gesetz, das die Krankenhäuser betrifft – das ist das Krankenhauszukunftsgesetz (KHZG) auf jeden Fall. Das Gesetz wirkt sich aber auch auf die Hersteller...
Der 26. Mai 2021 ist der Geltungsbeginn für die neuen Regeln in der Medizintechnik-Branche, die Medical Device Regulation. Der Branchenverband BVMed sieht...
Am 26. Mai 2021 wird die MDR in Kraft treten, nachdem der Geltungsbeginn infolge der Covid-19-Pandemie um ein Jahr verschoben wurde. Auch wenn die Pandemie...
Ein Medizinprodukt wie ein verlängerbarer Marknagel soll für viele Anwendungen geeignet sein und wird daher als Baukasten konzipiert. Diese Vielfalt gemäß...
Am 26. Mai 2021 tritt die EU-MDR in Kraft. Den hohen Aufwand, den die Medical Device Regulation erfordert, ist für viele kleine und mittlere Unternehmen kaum...
Die ISO 15223–1:2021* und ISO 20417:2021* nehmen Einfluss darauf, wie die Kennzeichnung von Medizinprodukten und ihren Verpackungen auszusehen hat und welche...
Erst der Zweck macht die App zum Medizinprodukt. TÜV Süd empfiehlt Entwicklern, Herstellern und Inverkehrbringern, sich im Zweifel am MDCG-Leitfaden zur...
Wie lässt sich bei Software als Medizinprodukt Cybersecurity gewährleisten? Eine Norm gibt es dafür nicht – wohl aber eine Reihe von Papieren, die...
Die Europäische Kommission hat eine neue Webseite eingerichtet, auf der alle notwendigen Informationen zur Registrierung von Wirtschaftsbeteiligten in Eudamed...
Die aktuelle Version der Norm ISO 14155:2020 liegt vor und Hersteller tun gut daran, ihre klinischen Prüfungen daran zu orientieren. Ein neuer Fokus betrifft...
Wahre Datenberge sind zu berücksichtigen, um gemäß den Vorgaben der kommenden Medical Device Regulation (EU MDR) zu sammeln und auszuwerten, was mit einem...
Veränderter Geltungsbeginn | Wegen der Umbrüche, die die Coronavirus-Pandemie weltweit verursacht, hat die EU-Kommission den Geltungsbeginn der Medical...
Seit 2017 sind die gesetzlichen Vorgaben für Medizinprodukte ein heißes Thema in der Medizintechnik-Branche: Denn mit der neuen, künftig EU-weit gültigen...
Anfang des Jahres ist das Gesetz zur Errichtung eines deutschen Implantateregisters in Kraft getreten. Das deutsche Institut für Medizinische Dokumentation...
Das Digitale-Versorgung-Gesetz (DVG) soll digitalen Gesundheitsanwendungen den Weg in die Erstattung durch Krankenkassen ebnen. Natalie Gladkov, Referentin...
Der Ulmer Medizintechnikhersteller Ulrich GmbH & Co. KG meldete im Januar, dass das Unternehmen die ersten MDR-bezogenen Audits abgeschlossen hat. Andreas...
Unter Eudamed.eu ist ein Beratungsunternehmen erreichbar, dessen CEO Richard Houlihan als IT-Experte an der Eudamed-Datenbank mitgearbeitet hat. Nun stellt...
Das aktuelle Korrigendum der Medical Device Regulation (MDR) legt fest: Wichtige Bestandsprodukte wie chirurgische Instrumente dürfen weiter unter den...
Das virtuelle Abbild von Produkten und Patienten, ihr digitaler Zwilling, kann die Entwicklung und Überwachung von Medizinprodukten unterstützen, erleichtern...
In-vitro-Diagnostika | Die EU-Kommission hat die Dekra Certification als Benannte Stelle nach der neuen EU-Verordnung für In-vitro-Diagnostika (IVD)...
Für die klinische Bewertung von Medizinprodukten werden mit der Medical Device Regulation (MDR) mehr eigene Daten erforderlich sein, da man sich nur noch...
Seit Juli 2019 beschreibt der Weißdruck der VDI-Richtlinie 2017, was Werkstoffanbieter und Medizinproduktehersteller unter Medical Grade Plastics verstehen...
Nach einem ersten Entwurf des Medizinprodukte-Anpassungsgesetzes-EU sind Sonderzulassungen für Medizinprodukte in Deutschland geplant...
GS1 Germany ist mit der Akkreditierung durch die EU-Kommission jetzt offizielle Zuteilungsstelle für die Unique Device Identification.
Als erste Benannte Stelle gemäß Medical Device Regulation außerhalb von Großbritannien könnte TÜV Süd seine Arbeit aufnehmen. Doch um ernsthaft anfangen...
Nach der Fusion von Medical Cluster und Fasmed vor zwei Jahren ist der neue Verband Swiss Medtech in einem stabilen Markt gut aufgestellt, doch das Thema...
Zulieferer und die EN ISO 13485 | Ein Qualitätsmanagementsystem, nach EN ISO 13485:2016 zertifiziert, ist für alle Beteiligten äußerst praktisch, sagt...
MDR – was noch zu beachten ist | Von den drei Jahren der Übergangsfrist bis zum Geltungsbeginn der MDR im Mai 2020 ist nur noch ein Jahr verblieben. Doch...
VDMA-Positionspapier zur EN ISO 13485:2016 | Im Mai hat die AG Medizintechnik im VDMA in ihrem Positionspapier die These aufgestellt, dass die EN ISO...