Gehirntumoren gehören zu den aggressivsten und tödlichsten Krebserkrankungen. Vor allem bei jungen Menschen zählen sie zu den häufigsten Tumorneuerkrankungen. Besonders gefürchtet ist das Glioblastom, das sich durch ein sehr rasches Tumorwachstum auszeichnet und sehr schwer zu behandeln ist. Mittlerweile weiß man, dass Gehirntumoren durch eine Vielzahl verschiedener Mutationen in Kombination mit äußeren Faktoren ausgelöst werden. Mutationen sind genetischen Defekte, die durch natürliche Fehler beim Kopieren von DNA oder durch die Aktivität von Krebsgenen entstehen oder andere Ursachen haben. Sie lösen bei gesunden Zellen schwerwiegende Veränderungen aus, die dazu führen, dass sie außer Kontrolle geraten und sich erstaunlich schnell teilen. In den vergangenen Jahren haben riesige Krebsgenom-Sequenzierungsprojekte Tausende von Mutationen katalogisiert, die in Patiententumoren gefunden wurden. Bis dato fehlte den Wissenschaftlern jedoch ein geeignetes Model, um die Wirkung dieser Mutationen im menschlichen Gehirn zu erforschen.
Krebsentstehung in der Petrischale
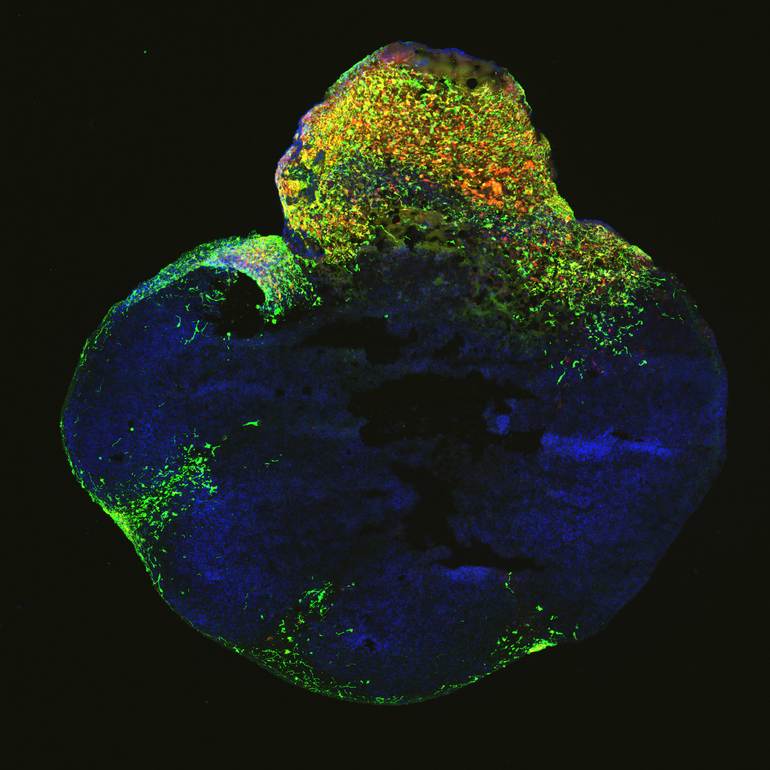
Die am IMBA – Institut für Molekulare Biotechnologie der Österreichischen Akademie der Wissenschaften erstmals entwickelten Gehirn-Organoide könnten nun auch für die Krebsforschung eine treibende Rolle spielen. Die Forschungsgruppe rund um Jürgen Knoblich hat kürzlich ein neues Modellsystem für Hirntumoren entwickelt. Das Novum: Die neue Technologie erlaubt es den Forschern, den Prozess der Krebsentstehung im Gehirn nun in der Petrischale nachzuspielen. Die Forscher können dadurch praktisch dabei zusehen, wie dem Organoid ein Tumor wächst.
„Diese kleinen Organoide reproduzieren einzigartige Aspekte des menschlichen Gehirns detailgetreu, wie zum Beispiel seine verschiedenen Zelltypen und Entwicklungsstadien. Sie erlauben uns daher, die Art und Weise, wie Tumoren entstehen, nachzuvollziehen und bieten ein System, um neue Therapien zu erproben,“ so Jürgen Knoblich, Interimistischer Wissenschaftlicher Direktor am IMBA und Letztautor der Studie. Die Forscher hoffen, mit Hilfe der Organoide zu unterscheiden, welche Mutationen Triebkräfte in Tumoren sind.
Organoide für eine personalisierte Krebsmedizin
Sie testeten dieses Prinzip mit einem Medikament namens Afatinib, das derzeit in klinischen Studien zur Behandlung von Glioblastomen eingesetzt wird. Und fanden heraus, dass nach 40 Tagen Verabreichung des Medikaments die Anzahl der Tumorzellen in jenen zwei Mutationskombinationen signifikant zurückging, in denen ein Molekül namens EGFR überexprimiert wird- denn Afatinib hemmt EGFR. Die Forscher wiederholten das Experiment mit vier zusätzlichen Wirkstoffen, die EGFR hemmen und derzeit in Therapien zum Einsatz kommen. Während ein Medikament namens Erlotinib die Anzahl der Tumorzellen signifikant reduzierte, waren die Effekte anderer Wirkstoffe minimal.
„Diese Ergebnisse zeigen, dass Gehirn-Organoide auch einen erheblichen Nutzen für die Krebsforschung beziehungsweise die öffentliche Gesundheit haben. Vor allem, weil es nun möglich ist, Organoide von Patienten mit Gehirntumoren herzustellen und daran die Wirksamkeit verschiedener Therapie-Kombinationen zu testen“, sagt Jürgen Knoblich.
www.nature.com/articles/s41592–018–0070–7