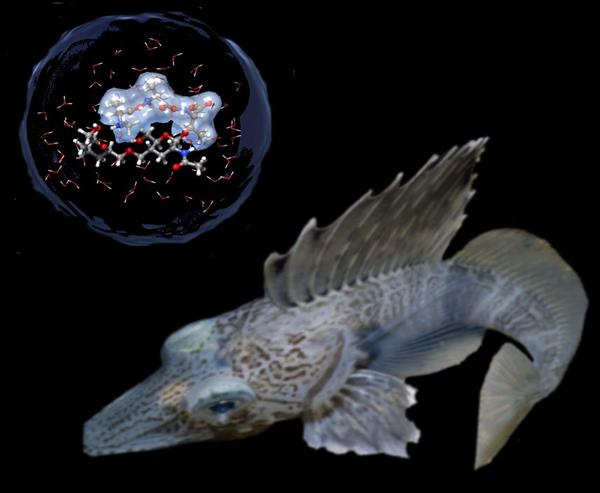
Selbst bei einer Bluttemperatur von 1,8° C sind antarktische Fische noch beweglich. Jetzt haben Forscher der RUB per Terahertz-Spektroskopie herausgefunden, dass ein Gefrierschutzprotein im Fischblut die Wassermoleküle in seiner Umgebung so verändert, dass ein Ausfrieren unmöglich wird und das Ganze flüssig bleibt.
Dabei besteht zwischen Protein und Wasser keine chemische Bindung – die Anwesenheit des Proteins genügt. Und das, obwohl der Gefrierpunkt für Fischblut bei ungefähr minus 0,9° C liegt. Schon vor 50 Jahren wurden besondere Gefrierschutzproteine im Blut dieser Fische entdeckt, die besser funktionieren als jedes haushaltsübliche Frostschutzmittel. Wie sie aber funktionieren, war bislang noch ungeklärt. Die Bochumer Forscher setzten ihre Spezialität ein, die Terahertz-Spektroskopie. Mit Hilfe von Terahertz-Strahlung lassen sich die kollektiven Bewegungen von Wassermolekülen und Proteinen beobachten. So konnte die Arbeitsgruppe schon zeigen, dass Wassermoleküle, die in flüssigem Wasser normalerweise einen ständigen Tanz aufführen und dabei immer neue Bindungen untereinander eingehen, in Anwesenheit von Proteinen geordneter tanzen – „aus dem Discotanz wird ein Menuett“, schildert Prof. Martina Havenith-Newen.
„Wir konnten sehen, dass das Protein einen besonders weitreichenden Einfluss auf die Wassermoleküle in seiner Umgebung hat, wir sprechen von einer erweiterten Hydrathülle“, erklärt Mitautor Konrad Meister. „Dieser Einfluss, der die Eiskristallisation verhindert, ist bei tiefen Temperaturen sogar ausgeprägter als bei Zimmertemperatur“, setzt Havenith-Newen hinzu. Um das Wasser dennoch zum Gefrieren zu bringen, wären tiefere Temperaturen nötig. Wenn man das Protein durch einen speziellen Boratpuffer deaktiviert, funktioniert der Gefrierschutz nicht mehr. In diesem Fall fanden die Forscher auch keine Änderung des Terahertz-Tanzes. Mit ihrer Beobachtung entkräfteten die Forscher die bisherige Annahme, dass eine einzige Bindungsstelle zwischen Anti-Freeze-Protein und Wasser für die Aktivität des Proteins verantwortlich ist. Mit der Untersuchung gelang zum ersten Mal der Nachweis eines direkten Zusammenhangs zwischen der Funktion eines Proteins und seiner Signatur im Terahertz-Bereich. Gemeinsam mit Kooperationspartnern aus den USA beschreiben die Forscher ihre Entdeckung in amerikanischen Chemiezeitschrift ‚Journal of the American Chemical Society‘.
Kontakt:
Prof. Dr. Martina Havenith
Teilen: