Qualitätsmanagement | Der Medizinproduktemarkt stellt hohe Anforderungen an Produzenten, damit zu keiner Zeit eine gesundheitliche Gefährdung bei den Nutzern der Produkte besteht. Die herstellenden Unternehmen unterliegen daher unter anderem einer Validierungspflicht, um geltende Qualitätsstandards zu sichern.
Dr. Iris Bruns Consense, Aachen
Die Validierung bei der Herstellung von Medizinprodukten ist eine komplexe, zeit- und kostenintensive Aufgabe – nicht nur für den Produzenten, sondern auch für alle Zulieferer, die ebenfalls die spezifischen Anforderungen erfüllen müssen. Moderne, auf GxP-Bestimmungen ausgerichtete Qualitätsmanagementsoftware unterstützt die regelkonforme Umsetzung. Dazu gehört unter anderem ein besonders aufwendiges Dokumentenmanagement, das eine revisionssichere Archivierung von Dokumenten sowie Prozessen und eine lückenlose Nachverfolgung sämtlicher Änderungen vorschreibt.
„Noch effizienter wird die Unterstützung, wenn die Software die Möglichkeit einer standortübergreifenden Nutzung bietet“, erklärt Dr. Alexander Künzer aus der Geschäftsführung der Consense GmbH, die sich auf Software für das Qualitäts- und Prozessmanagement spezialisiert hat. Mit der GxP-Version seiner Softwarelösung Consense IMS|QMS|PMS hat das Unternehmen ein vollständig überwachtes Managementsystem entwickelt, das bei der Einhaltung der jeweils gültigen nationalen und internationalen Standards unterstützt.
Von der standortübergreifenden Nutzung der Software profitieren Organisationen mit weit verzweigten oder sogar länderübergreifenden Standorten. Denn diese können die Vereinheitlichung ihres Qualitätsmanagements vereinfachen. Die große Herausforderung besteht für internationale Unternehmen unter anderem darin, alle Informationen – von einzelnen Dokumenten bis zu vollständigen Prozessbeschreibungen – einheitlich strukturiert und aktuell in allen im Unternehmen verwendeten Sprachen darzustellen. Dabei müssen oftmals außerdem länderspezifische Abweichungen, wie unterschiedliche Prozessabläufe, aber auch kulturelle Besonderheiten, berücksichtigt werden. Bei Unternehmen mit internationalen Standorten müssen darüber hinaus häufig Vorgaben umgesetzt werden, die im eigenen Land unbekannt sind. So sind beispielsweise börsennotierte US-amerikanische Unternehmen verpflichtet, ein Risikomanagementsystem nach Sarbanes-Oxley-Act aufzubauen.
Streng reglementierter Zugang für Lieferanten
Unternehmen aus dem Medizinprodukte-Sektor müssen sich zusätzlich ganz besonders auf ihre Lieferanten und deren Qualitätssicherungsmaßnahmen verlassen können. Unter anderem wir dies durch Lieferantenaudits überprüft. Auch hier vereinfachen standortübergreifende Nutzungsmöglichkeiten einer Softwarelösung die Qualitätssicherung.
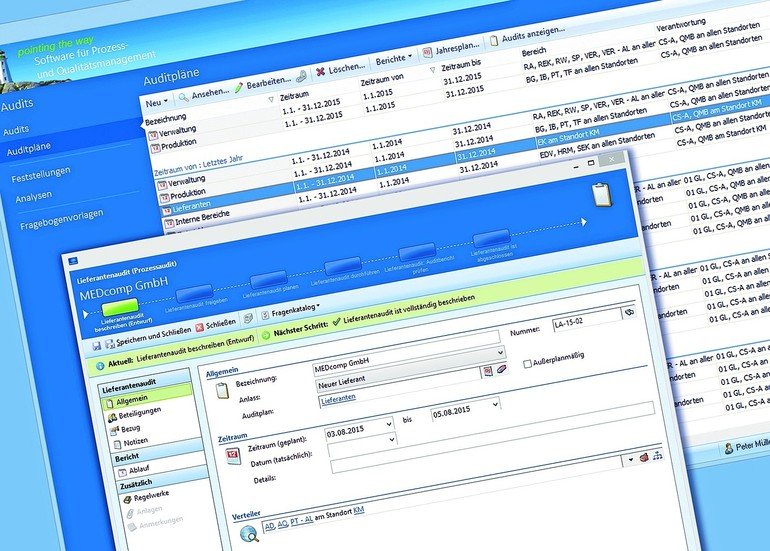
Die IMS|QMS|PMS|GxP-Lösung von Consense erlaubt externen Usern unter Anwendung eines dezidierten Rollen- und Rechte-Konzepts den Zugang zum System. So kann beispielsweise engen Geschäftspartnern das Lesen von ausgewählten Dokumenten und Prozessen gestattet werden. Sie können Einsicht in wichtige Informationen, wie allgemeine QM-Richtlinien oder notwendige Dokumente für eine Validierung, erhalten. Auch Projektordner zur gemeinsamen Nutzung durch beide Partner lassen sich anlegen. Das vereinfacht Lieferanten unter anderem die Vorbereitung ihrer Auditierungen und unterstützt sie darin, mit ihrem Qualitätsmanagementsystem die festgelegten Anforderungen des Medizinprodukteherstellers zu erfüllen.
Auch im Bereich der Schulungen und Unterweisungen im Zusammenhang mit Validierungen ist der standortübergreifende Einsatz der Software möglich. Hier bestehen für die Hersteller von Medizinprodukten ebenfalls strenge Auflagen für Schulungen zum Nachweis von spezifischen Kenntnissen zur Durchführung bestimmter Tätigkeiten und Prozesse. Unter anderem muss bei jedem Prozessschritt sichergestellt werden, dass die involvierten Personen die erforderlichen Schulungen absolviert und damit das nötige Wissen für die Durchführung ihrer Tätigkeiten haben. Oft ist es schwierig, alle fälligen Schulungen für alle betreffenden Mitarbeiter zu organisieren und die ordnungsgemäße Durchführung unter Kontrolle zu behalten, damit ein Prozess in Kraft gesetzt werden kann.
„Innovative Softwarelösungen für das Qualitätsmanagement, die auf die besonders anspruchsvollen GxP-Anforderungen zugeschnitten sind, gestalten gerade die aufwendigen Verfahren in der Medizinprodukteherstellung wesentlich effizienter“, erklärt Künzer. „Für uns war bei der Entwicklung unter anderem wichtig, technische Lösungen zu schaffen, die bei Bedarf eine standortübergreifende Nutzung erlauben und gleichzeitig die lokale Autonomie erhalten.“ Gerade weit verzweigte oder sogar internationale Unternehmen aus dem medizinischen Bereich haben damit viele Möglichkeiten, ihre Validierungsprozesse zu vereinfachen und zu beschleunigen. ■
Unsere Whitepaper-Empfehlung
Lesen Sie, warum Medizintechnikunternehmen ihre Testprozesse für die Validierung von Software optimieren müssen und wie sie dabei die Erfahrung der Automobilbranche für sich nutzen können.
Hier finden Sie mehr über:
Teilen: