Der 18. März war für ein Medizintechnik-Team in Berlin ein Freudentag. Daran konnte nicht einmal die Corona-Krise etwas ändern. Denn an diesem Termin endete ein mehrjähriges Projekt damit, dass ein neues, additiv aus Kunststoff gefertigtes temporäres Implantat das Okay von der Benannten Stelle bekam. „Wir sind den langen und harten Weg zur additiven Fertigung gegangen, und es gab schon ein oder zwei Momente, an denen wir ernsthaft überlegt haben, ob wir das Ganze lieber abbrechen sollen“, sagt Dirk Warmuth, Geschäftsführer der Eckert&Ziegler Bebig GmbH in Berlin, die das Implantat auf den Markt bringt. Aber das Unternehmen hat sich für das Durchhalten entschieden und damit den Grundstein für weitere Produktentwicklungen auf Basis der additiven Fertigung gelegt. Und es entstand sogar eine zusätzliche Idee: ein Kompetenzzentrum soll entstehen, in dem Medizinprodukte-Hersteller von den Erfahrungen profitieren können.
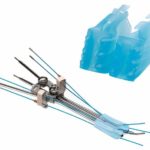
Das erste Produkt, das im März den „scharfen Blicken der Benannten Stelle standgehalten hat“, wie es Warmuth beschreibt, wird künftig bei der Bestrahlung von Tumoren am Gebärmutterhals eingesetzt. In der so genannten High-Dose-Brachytherapie werden Tumorzellen mit einer hohen Dosis von Strahlen behandelt. Die Strahlenquelle muss dafür ganz nah an das Tumorgewebe herangeführt werden, darf aber unterwegs das gesunde Gewebe nicht schädigen. Dafür setzt der Mediziner einen so genannten Applikator ein, der wiederum Führungen für flexible Nadeln enthält – in denen das strahlende Material zum Tumor geführt wird.
Inhaltsverzeichnis
1. Einfacher für den Mediziner – konventionell nicht machbar
2. 3D-Druck: Viele Informationen, aber nichts war übertragbar
3. Aussortieren, aussortieren, aussortieren
4. Der lange Weg zum Nachweis der Biokompatibilität
5. 3D-Druck und Qualität: Vollautomatisierung ist das Ziel
6. 3D-Druck ins Unternehmen integrieren – zuweilen eine Herausforderung
7. 3D-Druck und die MDR
8. 3D-gedrucktes Produkt zunächst gemäß MDD
9. Am Ende bot der 3D-Druck sogar mehr Freiheit als gedacht
10. Über das Netzwerk Med Print
11. Über den Anwender
Einfacher für den Mediziner – konventionell nicht machbar
Die Ausrichtung der Nadeln ist für den Erfolg entscheidend. Sie lässt sich über Komponenten beeinflussen, die bisher am Applikator – mit einem Werkzeug – in einer bestimmten Position befestigt werden. „Wir wollten zu einer für den Arzt einfacheren Lösung kommen. Wir wollten, dass er auch für ungünstig gelegene Tumore eine gut handhabbare Lösung bekommt und damit bis zu zehn Nadeln platzieren kann“, berichtet Thomas Osche. Er hat solche Lösungen als Produktmanager mit Ärzten diskutiert. Diesen hat die Idee gefallen – und da die angedachten Produkte konventionell nicht zu fertigen waren, kam der 3D-Druck ins Spiel.
Erste Prototypen waren schnell hergestellt. Aber diese waren zu groß, und für den ernsthaften Einstieg in die additive Fertigung würde viel mehr Know-how erforderlich sein. „Wir haben anfangs mit einer Projektdauer von etwa zwei Jahren gerechnet“, berichtet Bebig-Geschäftsführer Warmuth. „Damit waren wir aus heutiger Sicht etwas zu optimistisch.“
3D-Druck: Viele Informationen, aber nichts war übertragbar
Um das Projekt voranzubringen, stieß Michael Bräsel als Produktentwickler zum Team – mit Erfahrungen zum 3D-Druck in der Elektronik. Die größte Herausforderung aus seiner Sicht: Verfahren für den 3D-Druck und Werkstoffe gibt es zu Hauf, auch für Medizinprodukte, meist im Dentalbereich oder für Hörgeräte. Aber alle greifbaren Informationen waren nicht auf das geplante Produkt zu übertragen.
„Die Vielfalt an Materialien und Verfahren erschlägt einen im Grunde“, sagt Bräsel. „Daher haben wir nach einem externen Fachmann für den 3D-Druck gesucht.“ An dieser Stelle kam Christopher König ins Spiel, einer der Geschäftsführer der Nürnberger Dreigeist GbR. Der Dienstleister begleitet Entwicklungsprojekte mit additiver Fertigung in verschiedenen Branchen. „Es gibt schon heute unzählige Materialien“, sagt auch König. Da könne es leicht passieren, dass man sich verzettele. „Daher sind gerade am Anfang viele richtungsweisende Entscheidungen erforderlich. Wenn diese gefällt sind und man machbare Konzepte genauer verfolgt, dauert es im Schnitt drei Jahre, bis man in die Produktion einsteigen kann.“
Aussortieren, aussortieren, aussortieren
Am Anfang ging es also vor allem um das Aussortieren. Anforderungen und Erwartungen wurden definiert, dann entschieden, was alles nicht in Frage kommt – bis nur noch eine Handvoll übrig blieb.
Für Bebig kam es unter anderem darauf an, dass das Implantat biokompatibel sein sollte. Angaben der Materialhersteller halfen da nicht viel weiter. „Wenn ein Material als biokompatibel auf den Markt gebracht wird, ist es das natürlich auch“, so Produktentwickler Bräsel. Das sage allerdings nichts darüber aus, ob es auch noch biokompatibel ist, wenn es nach dem Drucken, dem Post-Processing und dem Sterilisieren vom Arzt aus seiner Verpackung geholt wird.
Der lange Weg zum Nachweis der Biokompatibilität
Einfache Tests zur Cytotoxizität, die an verschiedenen Entwicklungsvarianten gemacht wurden, ließen das Gros möglicher Ansätze wegen mangelnder Biokompatibilität ausscheiden. Aber selbst mit den heißen Kandidaten liefen laut Bräsel gefühlt unendlich vielen Analysen, um zu sehen, ob es überhaupt eine Chance gab, mit der gewählten Kombination aus Material und Verfahren zu einem biokompatiblen Produkt zu kommen. „Die Benannten Stellen wollen ja genau wissen, was im Produkt ist.“ Schließlich kam Bebig diesem Ziel aber nahe genug, um nachzuweisen, dass alle enthaltenen Stoffklassen bei der Anwendung des Medizinproduktes unter den Grenzwerten bleiben. „Um die additive Fertigung für Medizinprodukte besser nutzen zu können und die Biokompatibilität nachzuweisen, wäre es wirklich sehr wünschenswert, wenn die Hersteller zu ihren Materialien genauere Auskünfte liefern würden“, sagt Bräsel.
Neben der Materialfrage gab es einen weiteren zeitraubenden Aspekt: Klassische Verfahren der Qualitätssicherung helfen bei Teilen aus dem 3D-Drucker meist nicht. Damit jedes Produkt hält, was der Hersteller verspricht, muss daher der Prozess nach den Erfahrungen bei Bebig parametrisiert sein. Um es in Bräsels Worten zu sagen: „Es gibt im gesamten Prozess keine Unbekannte mehr.“
Auch das Post-Processing wurde genauer unter die Lupe genommen. Warum? „Wir sind auf geradem Weg zu einem vollständig digitalisierten Prozess, von den CAD-Daten oder sogar von den MRT-Daten eines Patienten bis zum fertigen Teil im Drucker“, sagt Christopher König von Dreigeist. „Und dann kommt sozusagen der Neandertaler ins Spiel, der ein filigranes Gebilde von der Bauplatte bricht und mit der Nachbearbeitung beginnt.“ Von da an werde es sehr schwierig, einen manuellen Prozess definiert zu führen. Eine Teilautomatisierung helfe, wenn es exakte Anweisungen gebe, was der Mitarbeiter zu tun hat. Nur so komme man zu reproduzierbaren und validierbaren Ergebnissen.
3D-Druck und Qualität: Vollautomatisierung ist das Ziel
„Diesen Weg sind auch wir gegangen“, sagt Eckert&Ziegler-Entwickler Bräsel. Dabei kam die Erfahrung, die sein Unternehmen mit der Automatisierung von Prozessen hat, dem Projekt zu Gute. „Wir nutzen jetzt einen marktgängigen 3D-Drucker für das DLP-Verfahren und haben für das Post-Processing die passenden Maschinen drum herum entwickelt.“ Das langfristige Ziel: Vollautomatisierung, um alles unter Kontrolle zu haben.
Das Direct Light Processing, kurz DLP oder Projektorbasierte Stereolithographie, basiert auf UV-Licht, das zum Polymerisieren eines Kunstharzes genutzt wird. Damit lassen sich kurze Fertigungszeiten erreichen, und es hat sich im Dentalbereich sowie bei der Herstellung von Teilen für Hörgeräte bewährt. Derzeit läuft die Fertigung auf einem DLP-Drucker bei Dreigeist in Nürnberg. Aber noch im Laufe dieses Jahres werden Wissen und Maschinen nach Berlin transferiert: Dort soll die Produktion dann bei Bebig in einem großen Reinraum stattfinden.
3D-Druck ins Unternehmen integrieren – zuweilen eine Herausforderung
Es geht also: Im Prinzip ist der 3D-Druck laut Dreigeist-Geschäftsführer König aus technologischer Sicht industrietauglich. Das Interesse daran nehme in der Medizintechnik erkennbar zu. Dennoch sei es – unabhängig von der Branche – zuweilen eine Herausforderung, diese Art der Fertigung in ein bestehendes Unternehmen zu integrieren.
Im Falle der Medizintechnik wollten die Benannten Stellen auch sehr genau erfahren, was ein Hersteller tue, um potenzielle Risiken zu minimieren. Der Eckert&Ziegler-Prozess wurde bei Dreigeist in Nürnberg durch die Benannte Stelle geprüft – deren Mitarbeiter haben sich das ganze vor Ort angesehen, bevor sie die Technische Dokumentation prüften. „Es hat uns überrascht, dass unser Partner Dreigeist vorab auditiert wurde“, sagt Eckert&Ziegler-Entwickler Bräsel, denn dieses Vorgehen sei eigentlich erst mit der MDR zu erwarten gewesen.
Dass additiv gefertigte Medizinprodukte auch für Benannte Stellen noch nicht zum Alltag gehören, bestätigt der TÜV Süd. „Bisher waren Medizinprodukte aus dem 3D-Drucker zumeist patientenspezifische Lösungen wie Zahnimplantate oder Orthesen, für die gemäß der Medical Device Directive MDD gilt, dass sie ohne CE-Kennzeichnung und ohne Mitwirkung einer Benannten Stelle auf den Markt kommen dürfen“, sagt Gregor Reischle, der bei TÜV Süd den Bereich Additive Manufacturing leitet. Lediglich für Produkte der Risikoklasse III seien Prüfungen vorgegeben, die das Qualitätsmanagement des Herstellers betreffen.
3D-Druck und die MDR
Gemäß Medical Device Regulation (MDR) werden künftig manche Produkte höherklassifiziert, was häufiger eine Zusammenarbeit mit der Benannten Stelle erfordern wird. „Und es wird genauer bezüglich der Adjustable Products unterschieden“, sagt Julia Hoyer, die bei TÜV Süd den Bereich Regulatory Affairs leitet. Wenn nur geringe Anteile eines Produkts patientenspezifisch angepasst werden, braucht das Basisprodukt eine CE-Kennzeichnung – mit allen laut MDR vorgesehenen Einzelheiten und der Beteiligung einer Benannten Stelle.
Noch gebe es für die technische Bewertung additiv gefertigter Medizinprodukte keine Standards. „Diese sind aber in Arbeit“, sagt 3D-Druck-Experte Reischle. Die branchenübergreifende DIN SPEC 70701, die generell Risiken bei der additiven Fertigung betrifft, sei ein erster Schritt in diese Richtung. Daraus abgeleitete Vorgaben für Medizinprodukte seien in Vorbereitung. „Das wird die Bewertung wesentlich erleichtern“, sagt auch Julia Hoyer.
3D-gedrucktes Produkt zunächst gemäß MDD
Während der Arbeiten für das Eckert&Ziegler-Projekt gab es solche allgemeingültigen Vorgaben noch nicht. Insgesamt hat das Team zwei Jahre und etwa neun Monate gebraucht, um die Produkte für die High-Dose-Brachytherapie fertigzustellen. Diese lassen sich nun durch ein Aufschnappen am Applikator anbringen und sollen zunächst in Europa vermarktet werden. Auch Asien sei ein interessanter Markt, auf lange Sicht die USA. „Da wir uns für die CE-Kennzeichnung gemäß MDD entschieden, uns aber gleich an den Vorgaben der FDA orientiert haben, sollte der Schritt nach Amerika kein Problem sein“, sagt Bräsel. Da Produktlinienerweiterungen geplant sind, ist in absehbarer Zeit auch schon ein Umsteigen auf die Zulassung gemäß MDR für Europa geplant.
Der Aufwand war allerdings insgesamt höher, als man das üblicherweise für ein einziges Produkt in Kauf nehmen würde. So ist der Einstieg in den 3D-Druck für Eckert&Ziegler wirklich nur der Anfang – weitere Produkte sollen folgen. Den Reinraum, in dem sie hergestellt werden, will Bebig-Geschäftsführer Warmuth für das geplante Kompetenzzentrum nutzen und mit seinen Fachleuten andere Medizinprodukte-Hersteller beraten. „Die strategische Entscheidung war, dass wir das Projekt erfolgreich zu Ende bringen und einen Trend setzen. Von unseren Erfahrungen können nun andere profitieren. Denn wenn man den 3D-Druck an sich im Griff hat, ist erst ein Teil der Arbeit getan.“
Am Ende bot der 3D-Druck sogar mehr Freiheit als gedacht
Dass die additive Fertigung tatsächlich interessante – auch ungeahnte – Möglichkeiten bietet, hat sich für Eckert&Ziegler Bebig schon beim ersten Produkt gezeigt. Es ist inzwischen nicht nur deutlich kleiner als der Prototyp und hat eine glattere Oberfläche. Auch seine Konstruktionsweise ist nicht mehr vom Drehen und Fräsen geprägt. Daher kann Produktmanager Osche den Medizinern künftig sogar noch mehr Freiheiten vorschlagen als anfangs gedacht: Das geht bis hin zu patientenindividuell angepassten Platzierungsmöglichkeiten für die Nadeln im Applikator. „Wir können die Patientendaten digital mit den Erfordernissen am Applikator abgleichen. Das hat sich so erst beim Umsetzen des Projektes gezeigt. Diese zusätzliche Freiheit ist hervorragend.“
Das CE-Kennzeichen ist erreicht – das ganze Ausmaß der Freude über das gelungene Projekt wird sich aber wohl erst zeigen, wenn über das Coronavirus hinaus auch wieder medizintechnische Themen eine größere Rolle spielen können.
Weitere Informationen
Über den 3D-Druck-Entwicklungsdienstleister
Über Ausbildungsangebote zur additiven Fertigung in der TÜV Süd Akademie
Über das Netzwerk Med Print
Speziell an kleine und mittlere Unternehmen, die Interesse am 3D-Druck haben, wendet sich das Netzwerk Med Print, das von Medical Mountains in Tuttlingen koordiniert wird. Darin haben sich Forscher, Medizinproduktehersteller und Zulieferer zusammengeschlossen. In der Phase I des ZIM-geförderten Netzwerkes haben 24 Partner eine Reihe von Handlungsfeldern definiert. Das Post-Processing der additiv gefertigten Teile ist eines davon.
Derzeit steht das Netzwerk an der Schwelle zur Phase II der Förderung – entsprechende Anträge sind in Arbeit. Drei Projektgruppen wollen demnächst
- geeignete Verfahren für die Reinigung von Teilen aus dem 3D-Druck entwickeln,
- Möglichkeiten der Oberflächenbehandlung aus loten, wobei das Anodisieren im Vordergrund stehen soll,
- besonders für die Medizintechnik geeignete Materialien auf der Basis von Kunststoffen, Metallen und Keramik entwickeln.
„Gerade bei den Materialien sehen wir noch sehr viel Potenzial“, sagt Dr. Manfred Kauer, der das Netzwerk bei Medical Mountains als Projektmanager betreut. Für PEEK und Titan gebe es bereits Quasi-Standards. Bei den Erfahrungen mit anderen Werkstoffen aber sei noch einiges aufzuholen. Unternehmen mit Expertise in diesen Fragen sind als weitere Partner im Netzwerk sehr willkommen, so Kauer – wobei Erfahrungen auch aus anderen Branchen wie der Automobilindustrie stammen können.
Das Potenzial des 3D-Druckes dürfe man nicht unterschätzen. „Es gibt aber durchaus Fälle, bei denen das Drehen oder Fräsen immer noch die wirtschaftlichere Alternative ist“, sagt Kauer. Daher sei gerade für KMU der Austausch mit anderen Unternehmen auf Augenhöhe ein guter Weg, um den Einstieg in eine neue Technologie wie die additive Fertigung zu bewältigen. Und gerade bei Fragen der Zulassung gebe es für die additive Fertigung noch viele Unwägbarkeiten.
Über den Anwender
Die Eckert & Ziegler Bebig GmbH in Berlin bietet Radiotherapie- sowie Brachytherapieprodukte an. Etwa 145 Mitarbeiter arbeiten in den Bereichen Technik, Physik, Medizinphysik, Vertrieb, Marketing und Verwaltung. Mit Niederlassungen und Tochtergesellschaften ist das Unternehmen in Europa, Asien und den USA vertreten. Bebig gehört zum Medizinsegment der Eckert & Ziegler AG, einem Anbieter von Isotopentechnologie für medizinische, wissenschaftliche und industrielle Zwecke. Das Kerngeschäft der Gruppe umfasst Krebstherapie, industrielle Radiometrie und nuklearmedizinische Bildgebung.